En los últimos años, la disfunción mitocondrial por metales pesados se ha consolidado como una de las hipótesis fisiopatológicas más relevantes para explicar la fatiga crónica, la inflamación persistente y la pérdida de resiliencia metabólica que observamos en consulta. Cada vez más pacientes presentan síntomas complejos y superpuestos —agotamiento físico y mental, dolor musculoesquelético difuso, alteraciones cognitivas e intolerancia al estrés— que no encuentran una causa clara en la analítica convencional.
Desde la perspectiva de la medicina integrativa y la Psico-Neuro-Endocrino-Inmunología (PNEI), estos cuadros no son procesos aislados, sino manifestaciones de una alteración bioenergética profunda. En el centro de esta alteración se encuentra la mitocondria, responsable de la producción de ATP, la regulación redox y el control de la señalización inflamatoria. Cuando su funcionamiento se ve comprometido, la célula pierde eficiencia y el organismo entra en un estado de inflamación de bajo grado sostenida.
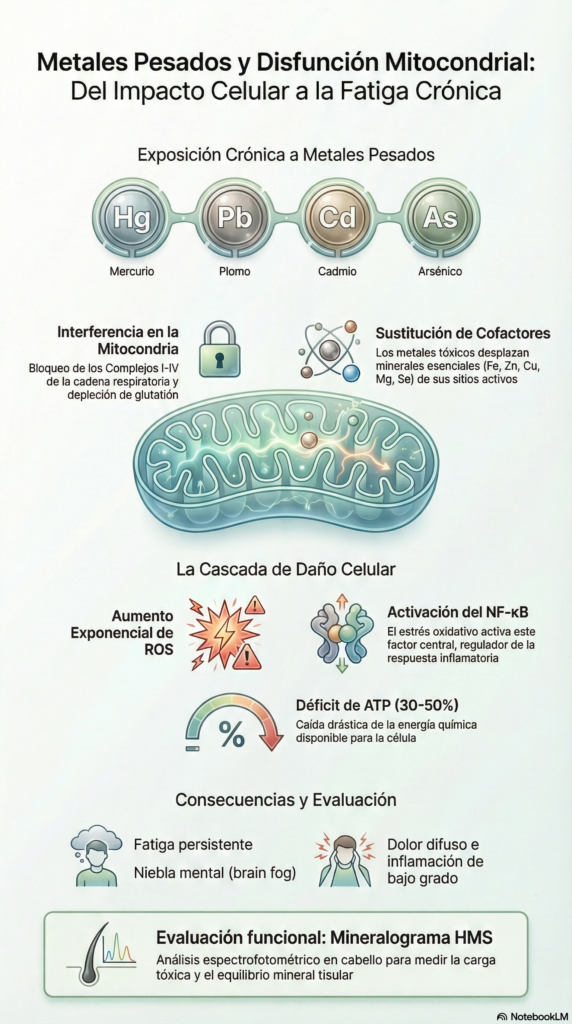
Uno de los factores menos explorados en este contexto es la carga corporal acumulada de metales pesados. Sustancias como mercurio, plomo o cadmio pueden interferir en la cadena respiratoria mitocondrial, desplazar minerales esenciales y generar un entorno de estrés oxidativo persistente. El resultado no es únicamente una disminución energética, sino una alteración sistémica que afecta al sistema inmune, endocrino y nervioso.
Comprender la relación entre metales pesados y función mitocondrial nos permite ir más allá del síntoma y abordar el terreno biológico de forma estratégica. Porque no se trata solo de tratar la inflamación, sino de restaurar la eficiencia bioenergética celular.
Cómo la disfunción mitocondrial por metales pesados altera la producción de energía celular
La disfunción mitocondrial por metales pesados no es un fenómeno abstracto, sino un proceso bioquímico concreto que compromete directamente la producción de ATP y el equilibrio redox celular. La mitocondria depende de un delicado sistema de transferencia de electrones —la cadena respiratoria— en el que participan minerales esenciales como hierro, cobre, magnesio y zinc. Cuando este equilibrio se mantiene, la célula genera energía de forma eficiente y controlada.
Sin embargo, metales tóxicos como el mercurio, el plomo o el cadmio pueden interferir en este proceso mediante un mecanismo conocido como competencia biometálica. Estos elementos desplazan a los minerales esenciales de sus sitios enzimáticos o bloquean directamente los complejos de la cadena respiratoria. El resultado es una disminución progresiva en la síntesis de ATP y un aumento compensatorio en la producción de especies reactivas de oxígeno (ROS).
Esta alteración bioenergética tiene consecuencias sistémicas. La célula entra en un estado de estrés oxidativo crónico, se activa el factor NF-κB y se promueve una señalización proinflamatoria persistente. Así, la pérdida de eficiencia mitocondrial no solo afecta al metabolismo energético, sino que se convierte en un motor silencioso de inflamación de bajo grado, fatiga crónica y vulnerabilidad inmunológica.
Desde una perspectiva integrativa, comprender este mecanismo permite entender por qué muchos pacientes presentan síntomas multisistémicos sin hallazgos relevantes en la analítica convencional: el problema no está en la estructura, sino en la bioenergética.
Mecanismos moleculares: cómo los metales pesados bloquean la cadena respiratoria mitocondrial
Para comprender la magnitud de la disfunción mitocondrial por metales pesados, es necesario descender al nivel bioquímico. La cadena de transporte de electrones (CTE), localizada en la membrana mitocondrial interna, es una estructura altamente especializada que convierte los electrones derivados de los nutrientes en energía utilizable en forma de ATP.
Metales como el mercurio (Hg), el arsénico (As), el cadmio (Cd) o el plomo (Pb) interfieren directamente en esta maquinaria mediante varios mecanismos complementarios.
Inhibición directa de los complejos respiratorios
Algunos metales pueden unirse a grupos sulfhidrilo (-SH) presentes en enzimas clave de la cadena respiratoria:
-
Mercurio y arsénico → inhibición del Complejo I
-
Cadmio → alteración de los Complejos II y IV
-
Plomo → disminución de la actividad del Complejo IV
Cuando estos complejos se bloquean, el flujo de electrones se interrumpe, disminuye la producción de ATP y aumenta la fuga electrónica, lo que genera radicales libres.
Depleción de glutatión y colapso del sistema antioxidante
El glutatión (GSH) es el principal antioxidante intracelular. Los metales pesados tienen alta afinidad por los grupos sulfhidrilo, lo que provoca su secuestro y disminución funcional.
Sin suficiente glutatión:
-
Aumenta el daño oxidativo
-
Se peroxidan lípidos de membrana (especialmente cardiolipina)
-
Se daña el ADN mitocondrial
Este escenario favorece una amplificación del estrés oxidativo.
Alteración del potencial de membrana mitocondrial
El daño estructural a la membrana mitocondrial interna genera una pérdida del gradiente electroquímico necesario para que la ATP sintasa funcione correctamente. La célula intenta compensar aumentando el consumo de sustratos energéticos, pero produce menos energía efectiva.
El resultado es un estado de ineficiencia metabólica crónica, característico de pacientes con fatiga persistente, intolerancia al esfuerzo y baja resiliencia al estrés.
Disfunción mitocondrial, estrés oxidativo e inflamación crónica de bajo grado
La disfunción mitocondrial por metales pesados no solo reduce la producción de energía; también altera profundamente la señalización inflamatoria celular. Cuando la cadena respiratoria se bloquea o se vuelve ineficiente, aumenta la fuga de electrones y se incrementa la producción de especies reactivas de oxígeno (ROS).
En condiciones fisiológicas, estas moléculas cumplen funciones de señalización. Sin embargo, cuando su producción supera la capacidad antioxidante —especialmente si el glutatión está disminuido— se activa una cascada inflamatoria sostenida.
Uno de los principales reguladores de esta respuesta es el factor de transcripción NF-κB, que se activa en presencia de estrés oxidativo. Su activación induce la expresión de citoquinas proinflamatorias como:
-
TNF-α
-
IL-1β
-
IL-6
Este estado de inflamación crónica de bajo grado no suele reflejarse en marcadores clásicos muy elevados,
pero sí genera un terreno metabólico alterado caracterizado por:
-
Fatiga persistente
-
Mayor sensibilidad al dolor
-
Disregulación inmune
-
Alteraciones metabólicas
Desde una perspectiva integrativa, la inflamación no es el origen primario, sino la consecuencia de una alteración bioenergética mantenida. Mientras la mitocondria permanezca ineficiente y el entorno redox desregulado, la señal inflamatoria continuará activa.
Por ello, en muchos pacientes con fatiga crónica o cuadros inflamatorios persistentes, abordar únicamente la inflamación sin considerar la función mitocondrial y la carga tóxica puede resultar insuficiente.
Evaluación funcional: el papel del Mineralograma en la disfunción mitocondrial por metales pesados
La evaluación convencional de metales pesados en sangre u orina suele reflejar exposiciones recientes, pero ofrece información limitada sobre la carga acumulada en tejidos y, sobre todo, sobre el impacto metabólico que esta carga genera en el organismo.
Desde una perspectiva funcional, no solo importa cuánto metal está presente, sino cómo está respondiendo el terreno biológico.
Aquí es donde el Mineralograma de Cabello (HMS) adquiere relevancia clínica. Este análisis permite observar patrones minerales acumulativos durante un periodo aproximado de 3–4 meses, ofreciendo una visión más amplia de la dinámica metabólica.
El valor del mineralograma no reside únicamente en detectar niveles elevados de metales, sino en interpretar las relaciones entre minerales esenciales, que pueden revelar vulnerabilidad mitocondrial y alteraciones redox.
Algunos indicadores especialmente relevantes incluyen:
-
Proporción Na/K → reflejo del estado adaptativo y del equilibrio neuroendocrino
-
Relación Zn/Cu → modulador inmunitario y antioxidante
-
Equilibrio Ca/Mg → excitabilidad celular y regulación energética
-
Déficits relativos de Fe, Zn o Se → mayor susceptibilidad a la interferencia por metales tóxicos
Cuando estos patrones muestran desequilibrios sostenidos, la mitocondria se vuelve más vulnerable a la competencia biometálica y al estrés oxidativo.
Es importante subrayar que el mineralograma no establece un diagnóstico médico por sí mismo. Su valor reside en integrarse dentro de una historia clínica completa y en servir como guía para intervenciones progresivas orientadas a restaurar el equilibrio mineral y mejorar la eficiencia bioenergética.
En el contexto de la disfunción mitocondrial por metales pesados, esta herramienta permite pasar de la sospecha clínica a una estrategia personalizada basada en el terreno metabólico real del paciente.
Conclusión: restaurar la bioenergética antes de apagar la inflamación
La inflamación crónica no puede entenderse aislada de la función mitocondrial. Cuando los metales pesados alteran la bioenergética celular, comprometen la capacidad adaptativa del organismo y perpetúan un estado de disfunción sistémica. Restaurar el equilibrio mineral y optimizar la eficiencia mitocondrial no es un abordaje accesorio, sino una estrategia central en medicina integrativa avanzada.
Cómo integrar esta evaluación en tu práctica clínica
Si en tu práctica clínica observas pacientes con fatiga persistente, inflamación crónica o síntomas multisistémicos difíciles de encajar en la analítica convencional, puede ser momento de ampliar la mirada.
Comprender la posible relación entre carga mineral, función mitocondrial y regulación inflamatoria permite diseñar intervenciones más precisas y personalizadas.
El Mineralograma HMS ofrece una herramienta de evaluación funcional orientada a interpretar el terreno metabólico y detectar patrones de vulnerabilidad bioenergética.
- Si eres profesional sanitario, descubre nuestras formaciones en mineralómica clínica aplicada y aprende a integrar esta herramienta en tu consulta. https://gheos.gheosnatural.com/
- Si eres paciente y deseas una evaluación personalizada, puedes solicitar información sobre el análisis HMS y su interpretación profesional. https://gheosnatural.com/mineralograma-para-humanos/
Restaurar el equilibrio mineral es un paso fundamental para recuperar resiliencia celular.
